Każdego roku w pełni lata podnoszony jest problem wykorzystania słomy. Dyskusje na ten temat zawsze są trudne. Uproszczeniem było stwierdzenie, że dotyczą tylko wartości nawozowej słomy i resztek korzeniowych. Równie ważne jest efektywne włączenie sporego zasobu węgla czyli energii i praktycznie wszystkich składników pokarmowych zakumulowanych w słomie w układ gleba – mikroorganizmy – roślina.
A jest to niemała masa organiczna. Dane pod względem ilości słomy produkowanej corocznie w Polsce są dość rozbieżne, zależnie od przyjętej metody obliczeń. W starszych opracowaniach jest to przedział 23 – 33 mln ton (podano za Pikuła 2015). Obecnie, na podstawie raportu „Biomasa w Polsce 2022/23” (magazynbiomasa.pl) można przyjąć, że potencjał słomy z Polsce wynosi około 34 mln t, z czego około 1/3 wykorzystywana jest jako ściółka w produkcji zwierzęcej. Pozostała część przeznaczana jest na cele energetyczne i nawozowe. Nie wchodząc w skomplikowane (często bardzo emocjonalne) rozważania na temat zagospodarowania słomy, skupmy się na zasobach pozostawianych na polu.
Znaczenie słomy należy rozpatrywać przynajmniej na czterech poziomach:
- Jest źródłem składników mineralnych (wszystkich, choć w różnych proporcjach). Teoretycznie, prowokując dyskusję, można przyrównać wartość żywieniową słomy do nawozów mineralnych, różnicując tylko szybkość uwalnia składników.
- Stanowi materiał wyjściowy do produkcji kwasów humusowych składających się na próchnicę glebową, której nie da się odbudować na bazie nawozów mineralnych. Nie oznacza to jednak, że nawozy mineralne nie stanowią wsparcia w całej sekwencji zdarzeń (etapowy rozkład i wtórna synteza). Wrócimy do tego za chwilę.
- Poprzez wpływ na zasoby próchnicy glebowej słoma kontroluje żyzność gleby odniesioną do właściwości fizycznych (struktura gleby w powiązaniu z właściwościami powietrzno-wodnymi, w tym – co jest kluczowe – kilkukrotny wzrost pojemności wodnej), chemicznych (dostępność składników mineralnych, pojemność sorpcyjna i zdolność buforowa gleby) oraz biologicznych, związanych z aktywnością mikrobiologiczną, z wszystkimi pozytywnymi skutkami.
- Pamiętajmy, że jedna tona odbudowanej próchnicy to, jako podaje prof. Pietr, trwałe związanie około 1,6 t dwutlenku węgla, co ma duże znaczenie ekologiczne.
Wartość żywieniowa słomy
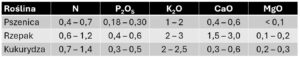
Skład chemiczny słomy wykazuje zróżnicowanie gatunkowe, związane z funkcjonowaniem określonej grupy rośliny (tab. 1).
Tabela 1. Skład chemiczny słomy (opracowano na podstawie danych różnych autorów)
Podane wartości stanowią zwykle punkt wyjścia w obliczeniach. Należy jednak pamiętać, że wartość żywieniowa słomy jest powiązana z dostępnością składników mineralnych w glebie w sezonie wegetacyjnym (im mniej zasobne stanowisko, tym mniejsza zawartość składników w słomie), a także z warunkami wzrostu rośliny. Chodzi o przemieszczanie (remobilizację) niektórych składników ze słomy do organów generatywnych wynoszonych z pola (kłosy, łuszczyny, kolby). Z tego powodu tak silnie zróżnicowane wartości dla azotu (tab. 1).
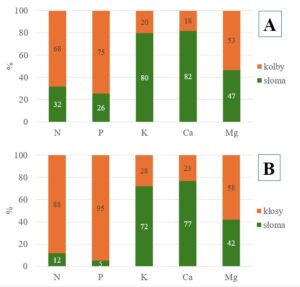
W tym miejscu dotykamy zagadnienia akumulacji poszczególnych pierwiastków w tkankach roślinnych. Słoma jest szczególnie zasobna w potas i wapń, natomiast w przypadku magnezu akumulacja kształtuje się na poziomie pobrania z ziarnem (ryc. 1). Można zaryzykować stwierdzenie, że wymienione składniki charakteryzują się dużą „stopą zwrotu”. Tak więc inwestycja w potas (ale także w wapń i magnez) nie jest całkowicie stracona. W przypadku azotu występuje dość duże zróżnicowania gatunkowe (największa akumulacja w słomie rzepakowej, w drugiej kolejności kukurydzianej).
Rycina 1. Akumulacja makroskładników w organach kukurydzy (A) i pszenicy ozimej (B), %; opracowano na podstawie danych podanych przez Grzebisza, UPP
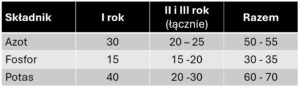
Bilansując składniki mineralne w skali pola lub gospodarstwa należy uwzględnić fakt, że słoma wykazuje działania następcze czyli rozłożone w czasie (tab. 2).
Tabela 2. Wykorzystanie składników pierwszoplanowych słomy w kolejnych latach po zastosowaniu
Słoma to przede wszystkim węgiel
Zawartość związków węgla w słomie kształtuje się na poziomie 35 – 55% C w s.m., zależnie od uprawianego gatunku. Dolny zakres dotyczy między innymi żyta i owsa, górny pszenicy, a pośrednie miejsce zajmują rzepak i jęczmień. Wspominam o tym nie przypadkowo. Słoma stanowi substrat do powstania próchnicy glebowej, w której dominującym pierwiastkiem jest właśnie węgiel. W skład słomy wchodzą między innymi celulozy i hemicelulozy (względnie łatwo mineralizowane) oraz ligniny (trudniej rozkładane).
Rozkładu słomy dokonują mikroorganizmy glebowe, dla których węgiel stanowi źródło energii, przy czym ze względu na złożony skład chemiczny konieczna jest obecność różnych grup mikroorganizmów. Naturalną konsekwencją dostarczenia słomy do gleby jest więc wzrost aktywności i liczebności mikroflory. W sprzyjających warunkach po wprowadzeniu do gleby rozdrobnionej słomy populacja mikroorganizmów może się podwoić, a są to wartości liczone w tonach. Proces rozkładu następuje w wyniku działania wielu enzymów, wydzielanych przez różne grupy mikrobów. Na przykład mineralizacja azotu obejmuje proteolizę (udział grzybów, promieniowców i innych bakterii Proteus sp., Bacillus sp. i Pseudomonas sp.) oraz amonifikację (dezaminazy produkowane przez inne bakterie glebowe). W efekcie powstają kationy amonowe (NH4+) jako pierwsze azotowe produkty mineralizacji materii organicznej.
Informacje te są potrzebne by zrozumieć, że funkcjonowanie organizmów glebowych wymaga stworzenia dla nich optymalnych warunków bytowania. Warunki te obejmują dostępność składników mineralnych (przejściowa konkurencja dla roślin) oraz odczyn.
Skład chemiczny słomy a dostępność azotu dla roślin – podstawy teoretyczne
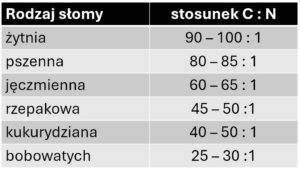
Składniki mineralne znajdują się w słomie w różnych formulacjach chemicznych, przy czym azot, fosfor i siarka występują głównie w formach organicznych. Stąd sygnalizowana w poprzednim akapicie złożoność reakcji uwalniania azotu z biomasy roślinnej czyli mineralizacji. To jednak nie jedyna grupa procesów. Równocześnie następuje bowiem immobilizacja azotu w biomasie mikroorganizmów czyli przejściowe związanie dużych ilości składnika w ciałach bakterii. Przejściowe oznacza, że po wyczerpanie się zasobów węgla część bakterii obumrze i ulegnie destrukcji, co będzie skutkowało powrotem azotu do puli dostępnej dla roślin. Trzeba podkreślić, że mineralizacja i immobilizacja zachodzą równocześnie. Dzieje się tak w każdej glebie, co nie dla wszystkich jest oczywiste. Rozważania na ten temat prowadzone przez naukowców dotyczą dominacji jednego z procesów. Pomijając czynniki abiotyczne (dostępność tlenu i wody, temperatura, odczyn i inne) i skupiając się tylko na składzie chemicznym wniesionej biomasy należy stwierdzić, że większa intensywność jednego w wymienionych procesów zależy od zawartości węgla (C) i azotu (N) w tkankach roślinnych, ściślej od relacji C:N (tab. 3).
Tabela 3. Relacja C:N oraz przybliżona zawartość azotu w słomie różnego pochodzenia (opracowano na podstawie danych innych autorów i badań własnych)
Generalnie im szersza relacja C:N i związana z tym mniejsza zawartość azotu w materiale organicznym (poniżej 1,2 % N w s.m. à 12 kg na 1 tonę) tym wolniejsza mineralizacja. Oznacza to dominację wiązania azotu mineralnego przez mikroorganizmy (immobilizacja) w stosunku do uwalnianego (mineralizacja). Powiemy zatem, że możemy spodziewać się przejściowego deficytu azotu dla roślin.
W literaturze przyjmuje się, że w sytuacji gdy relacja C:N zawiera się w przedziale 20-30:1 występuje równowaga między omawianymi procesami, przy szerszych wartościach dominuje immobilizacja, natomiast zawężenie wiąże się z promowaniem mineralizacji. Odnosząc się do wartości w tabeli 3 warto przywołać przefermentowany obornik, w którym wskaźnik C:N wynosi nieco powyżej 20:1.
Uwolnić potencjał słomy
Powracające dyskusje w okresie letnim można streścić następująco: azot czy wapno na słomę? Odpowiedź na tak postawione pytanie nie może być jednoznaczna i wprost, ponieważ zależy to od wielu czynników. Poniżej padną argumenty za i przeciw, lecz z pewną przekorą powiem, że jedno nie wyklucza drugiego, choć w pewnych warunkach połączenie obu zabiegów może być trudne, niekiedy wręcz niewykonalne.
1. Azot na słomę
Zamieszczony wyżej opis możliwych sekwencji zdarzeń stoi u podstaw podejmowanych decyzji przez rolnika. W doradztwie od lat lansowany jest pogląd, zgodnie z którym, pozostawienie słomy na polu musi wiązać się z zastosowaniem azotu mineralnego, po to by zawęzić relację C:N i tym samym przyspieszyć rozkład słomy. Oczywista jest konieczność wcześniejszego rozdrobnienia słomy. Należy jednak wziąć pod uwagę nie tylko sam fakt wprowadzenia słomy, lecz także jej skład chemiczny i uwzględnienie różnic gatunkowych (tab. 1).
Uogólniając należy przyjąć, że w przypadku klasycznych zbóż wskazane jest dostarczenie azotu mineralnego. Nie trzeba tego zwykle robić po przyoraniu słomy rzepakowej. Podkreślmy jeszcze raz – słoma odzwierciedla stan żyzności gleby na danym polu, a to znaczy, że ostateczna decyzja wymaga odpowiedniego rozeznania stanowiska. Może zdarzyć się, że po zastosowaniu dużych, zbilansowanych dawek nawozów azotowych uzyskamy zawartość azotu w słomie pszenicy ozimej na poziomie 1% N w s.m. (10 kg N w tonie, wartość bliska optimum dla równowagi mineralizacja/immobilizacja). Z kolei zawartość azotu w słomie z rzepaku ze względu na warunki stresowe w sezonie wegetacyjnym może kształtować się na poziomie znacznie poniżej podanej wartości krytycznej (1,2 % N w s.m.), co będzie rekomendacją do uzupełnienia zasobów azotu w formach mineralnych.
W ostatnich latach kwestia stosowania azotu mineralnego na słomę jest dyskutowana, ze względu na wątpliwości związane ze zbyt szybkim „spaleniem” materii organicznej i w związku z tym ograniczeniem próchnicotwórczej roli słomy. Szczegółowe wyjaśnienie problemu wymagałoby długiego wywodu akademickiego. Mówiąc najprościej – z definicji próchnica glebowa powstaje w wyniku procesów rozkładu biomasy organicznej (warunek konieczny) i późniejszej syntezy złożonych, co ważne – specyficznych dla środowiska glebowego – związków organicznych, z udziałem mikroorganizmów. W praktyce oznacza to, że materiałem do syntezy kwasów próchnicznych po czasie staną się także ciała obumarłych mikroorganizmów, których populacja zmniejszy się po rozłożeniu materiału energetycznego (słomy). Dlatego nie obawiałbym się stosowania azotu mineralnego na słomę, przyjmując zasadę: po przyoraniu słomy pszennej i żytniej powinno się wprowadzić około 5 – 7 kg N/t słomy, natomiast w przypadku jęczmienia, rzepaku i kukurydzy należy to zrobić tylko wtedy, gdy mamy do czynienia ze słabszym stanowiskiem lub w warunkach deficytowego nawożenia azotem danej uprawy.
2. Wapno na słomę
Dyskutowanym rozwiązaniem, także wśród naukowców, jest kwestia stosowania nawozów wapniowych na słomę. Problem nie jest nowy, lecz używane argumenty „za” uległy w ostatnich latach pewnym modyfikacjom. W środowisku kwaśnym niektóre mikroorgnanizmy glebowe włączają w metabolizm produkty rozkładu słomy i wykorzystują je w procesach fermentacji. W efekcie powstają kwasy organiczne (octowy, propionowy, mlekowy i inne) oraz etanol i aceton. Związki te razem z pojawiającymi się po rozkładzie lignin kwasami fenolowymi działają na rośliny fitotoksycznie. W niektórych badaniach zwraca się uwagę na to, że wymienione związki mogą wywoływać nie tylko chlorozy, lecz także upośledzenie rozwoju korzeni i zahamowanie podziałów komórkowych w tkankach nadziemnych młodych roślin. Zjawiskom takim sprzyja wilgotna jesień. Stąd zalecenia promujące utrzymywanie odczynu w zakresie obojętnego. W przypadku gleb kwaśnych (od lat nie wapnowanych) obligatoryjna musi być względnie szybka regulacja odczynu (dawki rekomendowane w zaleceniach IUNG), natomiast w stanowiskach lekko kwaśnych na granicy pH obojętnego wskazana jest aplikacja wapna, najlepiej węglanowego, w niewielkich dawkach (około 200-300 kg CaO/ha). Należy pamiętać, że wymienione zabiegi mają także na celu zwiększenie efektywności działania większości mikroorganizmów, dla których optimum funkcjonowania zawiera się w odczynie obojętnym.
Osiągnięcie pozytywnych efektów, o których mowa jest możliwe także z wykorzystaniem tak zwanych stabilizatorów odczynu gleby. Bardzo dobrym rozwiązaniem może być zastosowanie na słomę nawozu LUBOPLON CAL-MAG. Działanie tego nawozu przejawia się w wielu aspektach, co podsumowano na rycinie 2.
Rycina 2. Znaczenie LUBOPLONU CAL-MAG zastosowanego na słomę
Regulacja/stabilizacja odczynu a stosowanie azotu
W kontekście powyższych rozważań powstaje pytanie o łączenie regulacji/stabilizacji odczynu i aplikacji azotu. Generalnie w środowisku zasadowym (a takie powstanie po wprowadzeniu nawozu wapniowego) następuje ulatnianie azotu amonowego do atmosfery w formie amoniaku. Może więc „uciekać” zarówno azot wprowadzony do gleby z nawozem mineralnym jak i świeżo zmineralizowany. Stąd zalecenie by okres między regulacją odczynu i stosowaniem azotu był możliwie długi. Konieczne jest także oddzielenie obu zabiegów uprawką mieszającą klasyczny nawóz odkwaszający w glebie, po to by do minimum ograniczyć kontakt związków o charakterze zasadowym z azotem amonowym.
Zdecydowanie mniejsze niebezpieczeństwo strat azotu wystąpi w przypadku wykorzystania omówionego LUBOPLONU CAL-MAG, co wynika z formulacji chemicznych związków zawartych w granuli nawozowej (obecność siarczanów). Dlatego w stanowiskach lekko kwaśnych i obojętnych warto rozważyć zastosowanie właśnie tego produktu.
Zapamiętaj !
- Słoma jest cennym źródłem potasu dla rośliny następczej, lecz pod warunkiem odpowiedniego bieżącego nawożenia tym składnikiem. Stąd utrzymanie przynajmniej średniej zasobności w potas należy uznać za inwestycję w przyszłość, zarówno w kontekście produkcji plonu głównego jak i pobocznego (pozostającego na polu). Z tego powodu warto zajrzeć w zakładkę NAWOZY POTASOWE.
- Stosowanie słomy nie rozwiązuje problemu żywienia fosforem. Dlatego jeśli jedynym zabiegiem przed siewem rośliny następczej ingerującym w profil glebowy jest wymieszanie słomy konieczna jest także jednoczesna aplikacja szybkodziałającego fosforu, na przykład SUPERFOSFATU PROSTEGO.